5′-核苷酸的合成方法比较
2007-09-26 22:59:11 来源:生物技术通报 评论:0 点击:
5′-核苷酸在农业、食品和医药行业有着广泛的用途。尤其是在婴儿食品和医药领域的应用中,有着不可替代的功能。在婴儿食品中,作为婴儿食品的添加剂其可以明显提高婴儿的免疫能力,促进肠道的成熟,促进脂蛋白和多不饱和脂肪酸的合成,减少婴儿感冒和腹泻等疾病的发生,有利于婴儿的正常生长和发育。在医药领域,临床实验表明, 5′-核苷酸参与人体代谢,促进内脏器官改进和恢复,改善骨髓造血功能,可作为治疗癌症病毒的辅助药物,是一种非常重要的医药原料。5′-核苷酸可使白细胞过量增生,对于各种放射性物质或药物引起的白细
胞下降、非特异性血小板减少等症状有良好的疗效,也可用于急、慢性肝炎的治疗。
工业上和实验室已经有多种方法生产各种天然和非天然5′-核苷酸。归纳起来,主要有以下四种:
化学合成法、微生物发酵法,酶解法以及酶催化法。
1 化学法
化学法生产5′-核苷酸,主要是以核苷为原料进行磷酸酯化反应。一般常用的核苷磷酸化试剂主要是磷酸或者焦磷酸的活性衍生物,如磷酸的一氯和二氯衍生物,焦磷酸酰氯,双-对-硝基-苯焦磷酸等。要在核苷的5′位的羟基上导入磷酸基而得到5′-核苷酸,必须在进行磷酸化反应之前预先以适当的保护基保护核苷上核糖的2′, 3′位的羟基。一般可以采用异丙叉基、卞基、乙酰基或苯亚甲基等基团保护,然后等磷酸化完成后再脱去保护基。这种方法因采用了保护、去保护步骤使得反应整体产率下降。目前,在工业上己经实现了用P2O5或POCl3为磷酸化试剂,在少量水存在下,不用任何保护剂,核苷直接进行磷酸化反应,从而生成相应的5′-核苷酸,得到较高的产率。如以POCl3使肌苷,鸟苷,腺苷,鸟苷,尿苷磷酸化,其相应的5′-核苷酸产率分别为91%, 90%, 84%, 89%, 88%[1]。此方法也适用于许多非天然核苷酸的合成。但是,当底物包含对酸不稳定的基团时,此法效果不好。同时,此方法的直接产品5′-核苷酸极性强,提纯困难、耗时。一些POCl3的衍生物较POCl3更温和,如磷酸咪唑,磷酸三唑,磷酸羟基苯并三唑等。应用这种磷酸化试剂前,核苷中糖基上其它羟基的保护是必要的。这类磷酸化试剂引入的磷酸基中含有保护基团,极性较小,其提纯也比较方便。这类磷酸化反应中的主要问题在于除去保护基团所需条件剧烈。用b-取代乙基保护基可以解决这个问题,它可以在温和的碱性条件下发生b-消除而离去[2, 3]。但是,这种反应较难控制。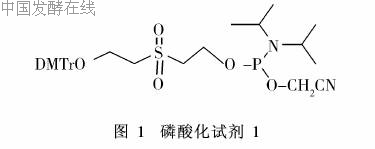
磷酸化试剂1(图1): (2-cyanoethyl)-2-[2′-O′-(4, 4′-dimethoxytrityl)oxy-ethylsulfonyl]ethyl-N,N-d-isopropylphosphoramidite既易于除去,又容易控制,但不足之处在于含有的亚磷酰胺基团不稳定[2]。人们还报道了许多此类保护基团,但是这些保护基都存在一定局限性,同时,保护和去保护步骤使得磷酸化产率降低。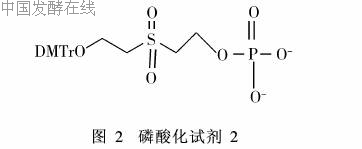
为避免这些缺陷,MichaelT和Vasu N开发了新型磷酸化试剂2(图2): 2′-O-(4, 4-dimethoxytri-tyl)ethylsulfonylethan-2-yl-phosphate。它可以使核苷中的伯醇和仲醇磷酸化,并能得到较高产率。此反应的一大优点是,磷酸化后的去保护步骤不会使整体反应产率降低,反而能起到促进作用,所以,整体反应产率可以达到80% ~95%[3, 4]。尽管人们开发出了许多化学合成5′-核苷酸的方法,但是,由于化学法有着各种局限,所涉及的试剂昂贵,且有一定毒性,生产成本偏高。因此化学合成法一般用于生产一些有特殊用途的5′-核苷酸,且仅限于实验室规模,工业化大规模生产有一定的难度。
2 微生物发酵法[7~9]
微生物发酵法生产5′-核苷酸,主要是利用微生物菌株的生物合成途径来生产5′-核苷酸。对于核苷这样的物质,比较容易透过微生物细胞,所以利用微生物发酵生产核苷比较容易。目前已有较成熟的发酵生产肌苷,鸟苷,黄苷,腺苷,尿苷,胞苷的方法。但是核苷酸极性较大,难于透过细胞膜,因此增加了菌体发酵生产核苷酸的难度。目前利用直接发酵法生产核苷酸仅适于生产5′-肌苷酸和5′-鸟苷酸。
2. 1 肌苷酸的发酵
2. 1. 1 微生物发酵法生产肌苷,再磷酸化生产肌苷酸 一般采用枯草杆菌、短小芽孢杆菌、产氨短杆菌作为肌苷菌种培养,利用温度分段控制的方法进行种子培养和发酵,生成肌苷,再采用离子交换树脂等方法将肌苷分离,然后通过化学法磷酸化得到5′-IMP。
2.1. 2 直接发酵生产5′-IMP 一般利用产氨短杆菌或谷氨酸产生菌进行诱变,得到的菌株肌苷最高产量为20~27mg/ml。在工业化生产中,主要利用产氨短杆菌突变株KY13105直接发酵生产肌苷酸。
2. 1. 3 发酵法生产腺嘌呤或5′-AMP,再采用化学或酶催化转化为5′-IMP。
2. 2 鸟苷酸的发酵
对鸟苷酸GMP的发酵来说,直接发酵生产GMP非常困难,野生微生物基本上不积累5′-GMP。要直接发酵生产GMP,不但要考虑反馈调节机制,还要控制微生物中的相关酶系,生产难度大。目前GMP采用的是发酵法和化学合成法相结合的方法生产,主要有以下四条路线:
2. 2. 1 发酵法生产AICAR(5-氨基-4-咪唑基羧基酰胺核苷),然后化学合成5′-GMP 在工业生产中,利用巨大芽孢杆菌B. MegateriumNo366发酵生产AICAR,AICAR的产量可以达到16g/L。以AICAR为原料化学合成5′-GMP产率可达到60% ~70%。
2. 2. 2 由发酵法生产鸟苷,再转化生产鸟苷酸 鸟苷产生菌一般是从腺嘌呤缺陷型肌苷产生菌出发筛选出来的枯草杆菌。目前高产菌株是枯草杆菌MG-1,产量达16g/L。鸟苷再由化学法或微生物酶法磷酸化生产5GMP。
2.2. 3 直接发酵法生产5′-GMP 利用诱变筛选得到的枯草芽抱杆菌可以发酵直接生产鸟苷酸。但是,由于目前GMP产量还太低,一些技术问题还没有解决,其大规模生产仍然存在困难。
2. 2. 4 发酵法生产黄苷或5′-XMP,然后酶法转化为5′-GMP。四条线路中,目前只有前面两条用于工业化生
产。
3 酶解法生产核苷酸
酶解法生产5′-核苷酸是历史最长、技术最成熟的生产方法。在日本,有近40%的核苷酸是以RNA为底物酶解得到的。利用桔青霉发酵生产出的核酸酶P1与从酵母中提取的RNA反应即可得到四种5′-核苷酸的混合物,将该混合物经离子交换树脂分离纯化可以得到四种核苷酸的纯品[10~13]。其流程如图3。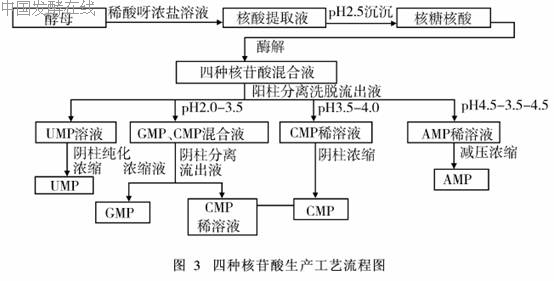
除桔青霉提取的核酸酶P1可酶解RNA外,还可以从麦芽根中提取磷酸二酯酶进行酶解反应[14, 15]。Olmedo等人利用固定床反应器研究了两种酶的动力学方程,发现上述两种酶具有很好的连续生产价值[16]。而利用固定化核酸酶生产5′-核苷酸的研究报道较多。除固定化酶生产核苷酸外,邵晶平等人利用膜反应器实现RNA连续水解生产核苷酸,为生产核苷酸提供了新的思路[17]。但是此法由于反应器的膜易堵塞而且膜反应器维护费用高,故不适用于大规模工业生产。
4 酶催化法
酶催化核苷磷酸化法,可用于制备许多5′-核苷酸,特别是一些具有高效药性而非自然存在的核苷酸,具有其他方法无法比拟的优越性。此法可以合成许多天然和非天然核苷酸,而且具有反应条件温和,容易控制,不需要保护基团,步骤简单,反应专一性强,副反应少,后处理容易等优点。目前,可用于5′-核苷酸合成的方法的酶主要是各种激酶。同时核糖磷酸转移酶和5′-核酸酶,酸性磷酸酶也被报道可用于核苷的5′位的单磷酸化。
4·1 激酶
激酶是一类可将来自ATP的磷酸基转移到别处的磷酸转移酶,按磷酸受体的性质不同可分为几个亚类,以醇基作为受体的亚类编号为EC2. 7. 1,其中许多酶都可以不同核苷为底物合成5′-核苷酸,反应式为:ATP+核苷=ADP+5′-核苷酸。激酶可用于生产多种5′-核苷酸,随着新药研究生产的需要,人们不断尝试用它们合成更多不同结构的核苷酸,这一努力也正得到越来越多的回报。以对脱氧胞苷激酶EC2. 7. 1. 74为例,这种酶的天然底物是脱氧胞苷,脱氧腺苷和脱氧鸟嘌呤,同时也催化1-b-D阿糖呋喃胞苷(Cytarabine,治疗成人急性粒细胞或单核细胞白血病的有效药物), 2′, 2′-二氟脱氧胞苷(Gemcitabine,吉西他滨,用于治疗非小细胞肺癌和胰腺癌)和2-氯脱氧腺苷(Cladribine,克拉屈宾,主要用于治疗临床上明显贫血、白细胞与血小板减少的活动性毛细胞白血病或与疾病相关的症状)等的5′位磷酸化[18]。因为许多核苷类药物在人体内起作用是通过形成其单磷酸盐,双磷酸盐直至三磷酸盐形式,而病体内催化核苷单磷酸化的酶浓度很低,所以探索在体外合成5′-核苷酸对提高药物效力有着十分积极的作用。并且激酶的磷酸供体不仅限于ATP,一些激酶也可以含其它磷酸基的物质如AMP,ADP, dGTP,甚至一些无机酸如焦磷酸,苯基磷酸酯等作为磷酸供体。了解各种激酶的结构,研究激酶对新的底物的作用,可以帮助我们将这些酶应用于新的核苷酸药物的合成生产。这种方法有着广泛的应用前景。
4·2 腺苷磷酸核糖转移酶APRT生产AMPAPRT(EC2. 4. 2. 7)全称是腺苷磷酸核糖转移酶,其一般反应式为:AMP+焦磷酸?腺苷+PRPP(5-磷酸核糖-1-焦磷酸)。此反应的逆反应即可用于AMP的合成。原料PRPP可以葡萄糖为底物在PRPP合成酶的作用下合成[19]。又由于化学合成的腺苷价格便宜,故用此法生产AMP成本较低。除APRT外, PPRT(嘧啶磷酸核糖转移酶),HGPRT(次黄嘌呤-鸟苷磷酸核糖转移酶)都是生物体内存在的磷酸核糖转移酶。在生物体内, PPRT以Oratate,尿嘧啶,胸腺嘧啶为底物,HGPRT以肌苷,鸟苷为底物合成其相应5′-核苷酸。但是,尚未看到这些酶用于生物体外的磷酸化的报道。
4·3 5′-核酸酶(5′-nucleotidase)5′-核酸酶(EC3. 1. 3. 5)的一般反应式为: 5′-核苷酸+H2O?核苷+磷酸,广泛作用于各种5′-核苷酸。此反应的逆反应即可用于多种单核苷酸的合成,这引起了人们的注意。JohnsonM A报道了在MgCl2,KCl存在下, IMP作为磷酸供体,以提纯的人类淋巴细胞质中的5′-核酸酶催化2′, 3′-双脱氧肌
苷的磷酸化,合成了其5′-单磷酸,并且此酶对2′,3′-双脱氧鸟苷也有作用[20]。之后人们研究表明细胞质中的5′-nucleotidase作用于多种核苷底物。这种酶对不同底物的作用效率由高到低依次为: (脱氧)肌苷, 2′, 3′-双脱氧肌苷, 6-氯嘌呤核苷, 6-羟胺基嘌呤核苷, 2, 6-双氨基嘌呤核苷,腺苷,胞苷,脱氧助间型霉素, 2′-脱氧腺苷[21, 22]。
4·4 酸性磷酸酶(Acid phospholase)
5′-IMP, 5′-GMP是呈味核苷酸,有非常大的需求量。传统的生产方法是用POCl3做磷酸化试剂的化学合成法和利用激酶的酶催化法。然而,化学法合成步骤繁琐,而激酶催化法需要利用ATP作为磷酸供体,增加了生产成本,这使得此法受到限制。酸性磷酸酶(EC3. 1. 3. 2)的一般反应式为:磷酸单脂+H2O?醇+磷酸,可作用于多种底物的水解,同时它的逆反应可用于催化磷酸转移反应。Ya-suhisaA等人发现M. morganiiNCIMB10466的提取物中有一种酶对核苷有磷酸化作用,并证明它是一种以焦磷酸为磷酸供体具有磷酸转移活性的酸性磷酸酶,其一般反应式为:核苷+焦磷酸→5′-核苷酸+磷酸,之后他们分离了M. morganii中控制其磷酸转移活性的基因,并诱发其突变后植入Escherichi-a coli中,结果筛选出一株富产酸性磷酸酶的变异株,对肌苷给出了85%的摩尔转化率[23]。但是因为这种酶既有磷酸转移作用也能催化磷酸水解,所以反应中必须控制条件。针对这一特点,人们诱变并筛选以催化磷酸转移为主导的菌珠,希望能抑制这种酶的水解作用,这些工作取得了一定成果[24]。现在,这一系列酶可从Salmonella typhimurium,Zy-momonasmobilis,M. morganii, shigella flexneri,prevo-tella intermedia得到[23]。这一发现为生产呈味核苷酸提供了新途径,由于磷酸供体焦磷酸便宜易得,使得此方法具有很大的发展空间。并且,这种酶对磷酸受体具有广泛的专一性,有可能可用于多种5′-核苷酸的合成。
5 总结与展望
5′-核苷酸用途广泛,与人们的生活息息相关,研究其不同的合成路径对医药,食品,农业等都有着非常重要的意义。目前已有的各种合成方法:化学合成法、微生物发酵法,酶解法以及酶催化法分别从不同的角度研究了5′-核苷酸的合成,但也各有利弊。化学法一般所需原料或催化剂较难得到,产率较低,后处理也麻烦,但此对底物核苷结构限制不大,具有广泛的作用范围;微生物发酵法,副产物少,成本低,但此法的应用受到微生物特性的很大限制;酶解法已成为制备各种天然核苷酸的经典方法;酶催化方法同时具有微生物法的产物单一,成本低的优点,又有化学法的作用范围广泛的特点,正受到越来越多的重视,此法的不足之处在于对酶的筛选工作量很大,同时酶的底物作用范围也有一定的限制。尽管5′-核苷酸的合成存在许多不足和困难,但5′-核苷酸的广泛应用正吸引着越来越多的工作者为之不断努力,我们有理由相信这些努力必将得到更多的回报。
相关热词搜索:5′-核苷酸
上一篇:纳他霉素发酵培养基及发酵条件的优化
下一篇:氢化可的松发酵液3次提取产物含量的研究
评论排行
- ·中国发酵企业数据库(4)
- ·(4)
- ·CoQ10高产菌株选育的研究进展(2)
- ·抗生素发酵工艺所用冷却塔的性能分析及处理(1)
- ·微生物菌种选育技术.rar(1)
- ·发酵生产染菌及其防治(1)
- ·赤藓糖醇发酵工艺研究(1)
- ·重组AiiA 蛋白可溶性表达及发酵条件优化(1)
- ·生物反应器设计软件_发酵罐绿色版(1)
- ·酵母粉、酵母浸粉的区别(1)
- ·雷帕霉素研究进展(1)
- ·透明质酸用途和行业概况(1)
- ·黄酒制作工艺(1)
- ·水解(酸化)工艺与厌氧发酵的区别(1)
- ·糖蜜酒精废液处理过程中产生的微生物蛋...(1)
- ·紫杉醇高产菌发酵产物的分离、纯化和鉴定(1)