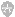The Research Progress of Succinic Acid Fermentatio
2007-10-19 18:57:05 来源:《生物工程学报》 评论:0 点击:
琥珀酸,学名丁二酸,是一种常见的天然有机酸,广泛存在于人体、动物、植物和微生物中[1]。作为一种重要的有机酸,琥珀酸在食品、化学、医药以及其他领域有广泛的应用,但其真正的潜力是作为大规模工业原料的应用。它可以取代很多基于苯和石化中间产物的商品,如果降低成本将可能有超过400万吨的市场容量[2]。但一直以不可再生的战略资源石油产品作为原料的传统琥珀酸生产方法导致了高价格和高污染,抑制了琥珀酸作为一种优秀的化学平台产品的发展潜力。而发酵法生产琥珀酸由于其高效率、环保性,以及原料的可持续利用性而受到一些研究工作者的推崇。美国能源部2004年发布的报告中(www. eere. energy. gov/biomass/pdfs/35523)将琥珀酸列为12种最有潜力大宗生物基化学品中的第一位。早在20世纪90年代初美国能源部就联合Argonne等四个国家实验室以及应用碳化学公司,投资700万美元联合进行琥珀酸的发酵和提取的研究(W-31-109-Eng-38)。2003年后又资助了多个琥珀酸发酵和分离的相关研究项目(DE-FG02-02ER83477,DE-FG02-00ER83034d等)。本文将就琥珀酸发酵菌种的十几年研究进展进行回顾、分析并展望了菌种的发展方向。
1 琥珀酸发酵菌种的多样性
琥珀酸是一些厌氧和兼性厌氧微生物代谢途径中的共同中间物。丙酸盐生产菌、典型的胃肠细菌以及瘤胃细菌能够分泌琥珀酸。据报道一些乳酸菌(Lactobacillus)也能在特定的培养基上不同程度地产生琥珀酸[3]。表1列出了已经报道的产琥珀酸菌种及其基本生理特性。由于天然菌株的产琥珀酸能力非常低,发酵产物多种多样,对糖或琥珀酸的耐受性比较差而使其基本不具有使用价值。因此必须运用生物工程技术对现有的菌种进行造。目前主要的研究进展集中在产琥珀酸厌氧螺菌(Anaerobiospirillumsucciniproducens),产琥珀酸放线杆菌(Actinobacillussuccinogenes)和大肠杆菌(Escherichia coli)等菌种上。
2 琥珀酸厌氧螺菌的研究进展
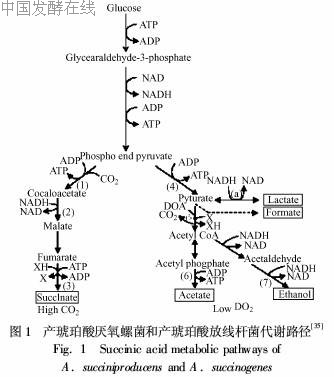
产琥珀酸厌氧螺菌(ATCC 29305)是从小猎犬的口腔中分离得到的一种革兰氏阴性严格厌氧菌,以葡萄糖乳糖为碳源发酵主产物为琥珀酸和乙酸,同时生成少量的甲酸、乙醇和乳酸[4]。一般认为产琥珀酸厌氧螺菌的代谢路径如图1所示。其中最主要的控制酶为PEP羧激酶、苹果酸脱氢酶、富马酸酶和富马酸脱氢酶。产琥珀酸厌氧螺菌发酵过程中,CO2浓度控制PEP的流向;在低CO2浓度时(0·1molCO2/mol葡萄糖)以乳酸作为还原的产物;而在高CO2浓度时(1mol CO2/mol葡萄糖)更多的流向还原臂,琥珀酸是主要的产物,仅有微量的乳酸产生。在最优条件下(pH6·2,高浓度CO2),琥珀酸的产量可以达到35g/L;有65%的葡萄糖被用于琥珀酸的生产[20]。在此情况下,可以检测到固定CO2的关键酶,PEP羧激酶浓度升高。此酶被进一步分离纯化,并进行了特性研究[21-24]。发现其满足米氏方程动力学模型,并且需要Mn2+、Co2+、Mg2+来表现最大活力。Laivenieks等人[25]进一步对编码PEP羧激酶的pckA基因进行了克隆、测序,发现产琥珀酸厌氧螺菌的PEP羧激酶和大肠杆菌的PEP羧激酶具有67·3%的同源性,79·2%的相似性。但在大肠杆菌中成功表达后却并未导致琥珀酸的产量升高。后,Jabalquinto等人[26,27]又运用定点突变的技术对此关键酶的动力学参数和催化活力中心进行了研究。Glassner等人[28]以产琥珀酸厌氧螺菌(ATCC29035)为出发菌株,通过筛选得到了比出发菌株更耐单氟乙酸钠的自发突变株FA-10(ATCC 55617)。此菌株的发酵产物中琥珀酸/乙酸的比例由大概4∶1提高到80∶1。此菌株对初始糖浓度最高耐受浓度为60g/L,最优初始糖浓度为30~50g/L。在最优发酵条件下琥珀酸的产量可以超过30g/L,得率超过70%,并有一定程度的丙酮酸积累。Samuelov等人[20]的研究结果表明,在最适条件下,产琥珀酸厌氧螺菌琥珀酸的产率可以达到120mol/100mol葡萄糖。最高浓度为65g/L。
研究结果一般认为产琥珀酸厌氧螺菌具有以下发酵特性[29-32]:
(1)可以利用的发酵底物比较广泛,可以以通常的碳水化合物为底物,例如葡萄糖、乳糖、甘油等。采用山梨糖醇为底物时会促进代谢向有利于产琥珀酸的方向代谢。
(2)厌氧发酵过程中,通入CO2对琥珀酸的代谢具有关键的作用,通入氢气可能会有利于琥珀酸的产生,最CO2/H2比例一般在95∶5。
(3)一般不能耐受高渗透压,最优底物葡萄糖浓度一般在20~80g/L之间,而且不能耐受高浓度
的琥珀酸盐。因此对分离步骤操作要求比较高。
(4)发酵最优pH一般为5·8~6·6,似乎较低
pH有利于琥珀酸的生产。一般为混合酸发酵,乙酸为主要的副产物。
3 产琥珀酸放线杆菌的研究进展
产琥珀酸放线杆菌(Actinobacillus succinogenATCC 55618)是从瘤胃中分离得到的一种革兰氏阴性新菌株,经16 S rRNA鉴定为巴斯德菌科放线杆菌属。它是一种兼性厌氧菌,能够利用多种碳源,并能够耐受高浓度的琥珀酸盐,而生长不受影响[5]。
以葡萄糖为底物时,发酵产生琥珀酸、乙酸以及少量的甲酸和乙醇。与产琥珀酸厌氧螺菌相似,CO2对琥珀酸的产量有很大影响,还原性底物有利于琥珀酸和乙醇的发酵产生。能够利用外源氢气作为电子供体,并以富马酸作为电子受体[33]。一般条件下琥珀酸的最后发酵含量可达50g/L,当使用100%氢气时,琥珀酸的产量可达110 g/L[33]。Guettler等人[33,34]以产琥珀酸放线杆菌130Z(Actinobacillus succinogenesATCC 55618)为出发菌株,筛选出对单氟乙酸抗性的自发突变株。此菌株发酵产物中的琥珀酸/乙酸比例高达85∶1;琥珀酸/甲酸比例高达160∶1。在最适条件下,此抗性株的琥珀酸产量可以达到80~110g/L,发酵时间48h,得率高达97%。此菌株的主要研究工作由MBI (MichiganBiotechnology Institute)完成。目前还没有其他研究单位的公开文献。从MBI对于此菌的产酸特性研究以及代谢方面的研究中总结,产琥珀酸放线杆菌中包含有EMP、PP途径的关键酶,而且其磷酸烯醇式丙酮酸羧激酶、苹果酸脱氢酶和富马酸酶的活性明显高于大肠杆菌K-12[34]。Kim等[102]克隆并在大肠杆菌中表达了此菌的磷酸烯醇式丙酮酸羧激酶,当敲除原菌的磷酸烯醇式丙酮酸羧化酶后,琥珀酸产率增加6·5倍。虽然研究较少,但此菌株是迄今为止报道的耐高糖和高盐的菌种,已经具备初步工业化生产的能力[35]。
4 大肠杆菌的研究进展
大肠杆菌在氧气缺乏的情况下,通常发酵糖或其衍生物为甲酸、乙酸、乳酸、琥珀酸、乙醇等产物[36]。通常情况下,大肠杆菌不会过量合成琥珀酸,因此其琥珀酸的产量很低,一般在0·12mol/mol葡萄糖。虽然大肠杆菌琥珀酸产量比较低,但因为其基础研究比较深入,能够采用各种分子生物学的技术对菌种进行改造,所以采用大肠杆菌发酵琥珀酸已经成为一个热点。
一般认为大肠杆菌的琥珀酸合成途径如图2所示,可以看到在大肠杆菌中产琥珀酸的途径比较复杂,可以多达6种[6]。综合文献的研究结果,可以概括为如下线索:
(1)以野生型大肠杆菌W1485为出发菌株:W1485能够利用大部分糖及其衍生物进行厌氧发酵。在LB培养基上生长旺盛,大约6~8h后到达稳定期。发酵产物为琥珀酸、乳酸、甲酸、乙酸和乙醇,
其中乙醇、乙酸、甲酸的产量最大,琥珀酸产量一般为0·15~0·2mol/mol葡萄糖[6]。Clark等人[6]通过插入抗性基因的方法构建了丙酮酸甲酸裂解酶pfl和乳酸脱氢酶ldhA的插入失活菌株NZN111 (F-pflA::Cam;ldhA::Kan)。NZN111不能以葡萄糖为碳源发酵生长,但可以以乳糖、果糖、甘露糖和海藻糖等为碳源发酵生成琥珀酸、乙酸和乙醇。Stols等人[37,38]发现,在大肠杆菌突变株NZN111中,表达Ascaris suum苹果酸酶能够使其生长恢复,琥珀酸的得率提高到0·39mol/mol葡萄糖,琥珀酸是主要的发酵产物;进一步的研究发现,在NZN111中表达NAD+依赖的大肠杆菌苹果酸酶后几乎进行单一的琥珀酸发酵,最优条件下发酵琥珀酸的得率能够达到1·2g/g葡萄糖。Charterjee等[39]对NZN111在含有卡那霉素的琼脂平板上培养后筛选到了能够重新发酵葡萄糖的自发突变株AFP111。AFP111能够发酵葡萄糖产生琥珀酸、乙酸和乙醇;并且能够利用外源氢为还原剂。当使用100%的CO2时,琥珀酸的产量可以增加到45g/L,生产能力可以达到1·6g/(L·h),得率可达到99%。
通过对AFP111的进一步研究发现其自发突变位置在编码PEP转移酶的基因ptsG,对于许多大肠杆菌和产乳酸杆菌的ptsG基因突变后都能够导致琥珀酸的产量上升[39]。Vemuri等人[40]进一步将编码Rhizobium etli丙酮酸羧化酶基因的质粒转移到AFP111中(AFP111/pTrc99A-pyc),通过IPTG诱导表达后,导致了琥珀酸产量的进一步提高。经过测定发酵过程中的酶活力发现,在AFP111有氧生长时,葡萄糖激酶和异柠檬酸裂解酶的活力上升。因此推测在AFP111中,存在两种葡萄糖的转运体系,并且乙醛酸循环占有一定比例。通过对AFP111/pTrc99A-pyc的发酵条件研究发现,在两步法培养(即先有氧培养,然后无氧发酵产酸)中转换时间的选择对其产酸具有决定作用。在最适的转换条件下(即溶氧浓度开始下降,但仍为90%时),琥珀酸的最终浓度可达到99·2g/L,得率为110%,生产能力1·3g/(L·h)[41]。
(2)Pan等人[42]以大肠杆菌W3110作为受体菌株,构建了乙酸和乳酸形成缺陷的双重突变株SS3(W3110pta::Tn10ldhA::Kan)。SS373大肠杆菌能够在葡萄糖培养基上厌氧条件下生长,因为它可以产生乙酰辅酶A,而大肠杆菌NZN111却不能。在两步法培养中,琥珀酸和丙酮酸是主要的发酵产物。当使用非PTS糖类发酵时,可以发酵产生几乎纯的琥珀酸。Lee研究组[43]最近发表了一篇采用将大肠杆菌和M.succiniciproducens基因组进行比较,从而识别提高大肠杆菌琥珀酸产量的关键基因的方法。依照此方法识别出了ptsG、pykF、sdhA、pykA、mqo和aceBA等关键基因。虽然全部敲除这些基因并没有导致琥珀酸的增产,但通过这些基因的组合,确实找到了ptsG、pykF、pykA的组合,基因敲除后,琥珀酸的产率可以提高7倍。
(3) Millard等人[44]通过在大肠杆菌JCL1208中过量表达PEP羧化酶,可以使其产量提高3·5倍,但过量表达PEP羧激酶却没有任何效果。Gorkan等人[45]通过在大肠杆菌JCL1242中表达Rhizobium etl的丙酮酸羧化酶基因发现,pyc的表达不影响糖的消耗速率和细胞的生长速率。在无氧条件下,pyc的表达使琥珀酸的产量提高了2·7倍,同时乳酸的得率明显下降。
(4) Rice大学San研究组最近连续发表多篇论文[46-49]及专利[50,51]论述了一系列大肠杆菌产琥珀酸研究。由于有氧条件下大肠杆菌具有高代谢速度和产物生成的优点,首先他们对大肠杆菌进行了基因工程改造以适应有氧发酵的条件。通过sdhAB、icd、poxB、ackA-pta、iclR等5个基因的敲除可以实现对有氧条件下乙酸代谢副产物的消除以及乙醛酸循环的激活,从而使琥珀酸成为主要的发酵产物。
但仍旧有相当量的柠檬酸和异柠檬酸发酵产生[47]。以sdhAB、poxB、ackA-pta、iclR四个基因敲除菌为平台,进一步通过ptsG基因敲除和PEP羧化酶的表达将有氧发酵产琥珀酸的得率提高到了理论值1mol/mol葡萄糖[49],从而显示了大规模有氧生产的潜力。
厌氧情况下,其主要采取的策略为通过基因缺失来消除代谢副产物的生成。首先发现在adhE、ldhA双缺失菌SBS110MG中表达丙酮酸羧化酶能够大幅度提高琥珀酸的得率到1·2mol/mol葡萄糖[48];他们通过进一步引入arcA、ack-pta、iclR基因缺失构建一系列菌株,发现在以上5个基因缺失菌SBS660MG中共同表达柠檬酸合成酶和丙酮酸羧化酶可以将厌氧琥珀酸的得率提高到接近理论值的1·7mol/mol葡萄糖[46],同时可以在24h内完全利用18g/L的葡萄糖。其在厌氧条件下的实验设计具有很高的理论价值,但在所有的实验中均采用了一种大接种量的接种方法(OD600=20)。在比较高的接种量下可以部分克服基因工程菌生长缓慢的缺点,但具体到工业化可能还需要做很多的工作。关于以上设计为何会导致高琥珀酸得率的理论问题,他们主要认为除了减少代谢副产物的消耗外,以上基因操作还使细胞内的可利用还原型NADH增加,从而有利于需要更多还原力的琥珀酸发酵[50]。
(5)其他重要菌株的研究进展:除了以上所详细描述的菌种以外,Lee SY等[12,52,53]连续发表了有关产琥珀酸新菌种Mannheimia succiniciproducensMBEL55E的多篇论文。此菌株为兼性厌氧革兰氏阴性菌,在pH6·0~7·5时生长良好。厌氧发酵产生琥珀酸、乙酸、甲酸的比例为2∶1∶1。之后,他们进一步对此菌种的PEP羧激酶进行了克隆、测序和特性研究[54],并且在2004年对此菌株进行了全基因组测序以及基因组规模的代谢通量分析和代谢特点研究[55]。研究结果发现,此菌株非常适应CO2环境,以富马酸作为电子受体代谢;其主要产生琥珀酸的途径为TCA循环的还原臂(CO2对PEP反应成为OAA的羧化步骤非常重要)以及甲萘醌系统。这种代谢特点非常有利于高产琥珀酸。虽然此菌的总体产量和得率都不高,但能够利用木质纤维素水解液以及乳清和玉米水解液等多种碳源。以木质纤维素水解液为碳源时批培养的琥珀酸最后浓度及得率分别为11·73g/L和56%,生产能力1·17 g/(L·h);连续培养的琥珀酸得率为55%,生产能力3·19g/(L·h)[12,52]。连续培养条件下的生产能力是目前报道的最高值,显示了良好的应用前景。除了细菌之外,许多研究者也对真菌的产琥珀酸特性作了研究。苹果酸产生菌Aspergillus spp.能够在生产苹果酸的同时分泌占总酸大约25%的琥珀酸[56]。Penicillium simplicissimum能够发酵葡萄糖在有氧和厌氧条件下产生少量的琥珀酸,最高产酸速率为0·063g/(g DW·h)[57]。虽然琥珀酸产量比较低,但由于其能够在厌氧条件下产生单一的发酵产物,以及揭示了菌球形成和产酸的关系等原因,真菌产琥珀酸也必将是一个非常有前途的研究领域。
5 菌种研究的分析和展望
对于研究比较多的产琥珀酸厌氧螺菌(ATC29305,ATCC 53488,ATCC 55617),共同存在的工业生产中的问题是:1·需要严格的厌氧环境,甚至用水都必须经过脱气处理,这在工业生产中难以实现。
2·需要的营养条件比较复杂,往往需要添加比较昂贵的氮源,因此会造成成本的升高,也会给后提取工艺增加困难。3·菌种普遍不能耐高渗透的盐和酸因此必须采取原位分离的技术,这也为工业生产带来困难。因此必须改变菌种的严格厌氧特性和耐粗放的发酵环境,而达到这样的目的还需要付出很大的努力。产琥珀酸放线杆菌ATCC 55618的突变株是迄今报道的产琥珀酸最高的菌株,可以达到110g/L,而且能够耐一定浓度的盐溶液,具备了初步工业化生产的能力。本实验室初步研究了产琥珀酸放线杆菌ATCC 55618,并对其发酵条件进行了研究。发现此菌种的营养要求比较复杂,而且在最优条件下38发酵产酸最高11·49g/L。可以看到这个数据和报道的数据差距比较大。通过选育单氟乙酸抗性突变株,可以进一步验证菌株的产酸能力。而且由于对此菌株的相关研究很少,因此有必要对其生理状态以及发酵特性进行进一步的研究。在此基础上,将利用基因工程技术结合代谢工程的方法来确定最优的发酵代谢路线,以及反应中的关键基因和酶。大肠杆菌是目前最有潜力的产琥珀酸发酵菌株,研究也取得了上述的众多进展。目前唯一公开报道的进行产琥珀酸中试的发酵菌株就是大肠杆菌。但大肠杆菌同样面临许多的问题。最主要的就是大肠杆菌厌氧发酵比琥珀酸生成效率相对较低[最高1·3g/(L·h)],通常进行混合酸发酵,以及不能耐高浓度糖发酵等。
为了获得发酵菌株的全面性能改进,可以预计单独依赖对某个具体基因或途径进行考察的传统还原论方法很难获得更大的进展,而必须通过以各种组学的合理联用,以及计算机辅助的菌株设计为特征的系统生物学的方法。目前已经有了许多基于组学规模的代谢关键途径或靶点识别的研究进展[43,58],可以预计系统生物学方法必将在琥珀酸菌株的改良中发挥更重要的作用。
相关热词搜索:琥珀酸
上一篇:发酵法生产多不饱和脂肪酸的研究进展
下一篇:花生四烯酸发酵动态代谢通量分析模型
评论排行
- ·中国发酵企业数据库(4)
- ·(4)
- ·CoQ10高产菌株选育的研究进展(2)
- ·抗生素发酵工艺所用冷却塔的性能分析及处理(1)
- ·微生物菌种选育技术.rar(1)
- ·发酵生产染菌及其防治(1)
- ·赤藓糖醇发酵工艺研究(1)
- ·重组AiiA 蛋白可溶性表达及发酵条件优化(1)
- ·生物反应器设计软件_发酵罐绿色版(1)
- ·酵母粉、酵母浸粉的区别(1)
- ·雷帕霉素研究进展(1)
- ·透明质酸用途和行业概况(1)
- ·黄酒制作工艺(1)
- ·水解(酸化)工艺与厌氧发酵的区别(1)
- ·糖蜜酒精废液处理过程中产生的微生物蛋...(1)
- ·紫杉醇高产菌发酵产物的分离、纯化和鉴定(1)