1 引 言
随着人们对健康环保纺织品需求的增加以及各国政府对环境保护强制力度的加大,在纺织印染行业中一种新型的纺织助剂———生物酶制剂的应用逐渐发展起来。目前,一种基于果胶酶的新型纺织生物助剂正在应用推广中,它主要用于棉、麻的前处理工艺。由于纺织企业多数对果胶酶的生物特性不甚了解,在工艺应用过程中缺乏相应的检测手段,使其推广受到限制。酶活力(活性)是衡量酶生物活性及含量的重要指标,因此,建立适用于纺织行业的果胶酶酶活检测方法,是十分迫切和必要的。
2 果胶酶的酶促作用机理
果胶酶是一类复合酶,是指分解果胶质的多种酶的总称。我们测定的酶活值通常是这一类复合酶协同作用的综合结果。果胶酶可分为两大类:解聚酶和果胶酯酶。解聚酶主要是通过水解作用和反式消去作用,切断果胶和果胶酶分子α-1,4糖苷键,将果胶分子降解为小分子。果胶酯酶的作用是使果胶分子中的甲酯水解,最后形成果胶酸。
果胶质主要是由D-半乳糖醛酸以α-1,4糖苷键连接形成的直链状聚合物。部分D-半乳糖醛酸上的羧基被甲醇酯化、形成甲酯,或被一种或多种碱部分或全部中和。果胶质在植物的细胞组织中起着“粘合”作用,在棉纤维的初生胞壁中,果胶质含量约占9%,而麻纤维则更高。
通过果胶酶的作用,将果胶质降解为小分子物质,从纤维中游离出来,可使与其粘合在一起的其它杂质(如蜡质、蛋白质、灰份等)与纤维素彻底分开,达到棉精炼或麻脱胶的目的。
对于纺织行业,需要的是将果胶催化水解成可游离出纤维的、小分子物质的果胶酶活性(力),因此,主要测定解聚酶的活力。解聚酶对果胶分子的酶促催化作用表现为,每切断一个果胶分子的α-1,4糖苷键,就会形成一个还原性醛基。通过测定这些还原性醛基生成的量,即可判定解聚酶的酶活力。
3 测定酶活力(性)的基本原理
酶作为一种生物催化剂,其酶活力值是与其催化效率及有效(即有生物活性)酶的含量相关的。酶活力是酶在单位时间内将底物转化为反应产物的能力,以U(mol/时间)表示,底物即是酶催化的反应物。通常,酶制剂的活力是以U/g酶制剂(或U/mL酶制剂)表示,把酶制剂的量和活力联系在一起,称为“比活力”。在特定条件下,通过测定单位量的某种酶制剂在单位时间内催化足够量底物生成反应产物的量,即可测出此酶制剂的比活力。
根据酶促反应动力学的米氏学说,从酶被底物饱和的现象出发,按照“稳态平衡”假说的设想,可推导出如下公式:
产物生成速率=k3[总酶][底物]/([底物]+km)(1)
式中: [总酶]———酶的总浓度(mol/mL);
[底物]———底物浓度(mol/mL);
k3———在酶促反应的第二步,形成最终产物的速率常数;
km———米氏常数(mol/mL),其值是当酶反应速率达到最大反应速率一半时的底物浓度。
要估计[总酶],首先要固定所有可控制的独立变量,如pH值、温度等。
当[底物]>>Km时,底物对反应速率的影响可忽略(酶饱和),酶促反应达到最大反应速率Vmax,其结果是:
产物生成速率=k3[总酶]=Vmax=U
U就成为总酶量的一种测量。因此,可以通过测定U来反映酶制剂中有效酶蛋白的含量。
4 果胶酶酶活的测定方法概述和比较
测定果胶酶酶活的方法有很多,但基本上都是利用酶促分解果胶产生的粘度下降或生成的还原性醛基来测定果胶酶酶活。这些方法概括起来主要有粘度降低法、滴定法和分光光度法3种。本文分别选取一种较典型的测定方法加以介绍。
4.1 粘度降低法
4.1.1 原 理
果胶溶于水后形成粘稠状溶液,其粘度和溶解度与其聚合和酯化程度有关。可以利用果胶的这种性质,测其酶活力。即在一定温度、酶浓度下和一定反应时间内,测定标准果胶溶液粘度的降低率。
4.1.2 操作方法
浴中保温10min后,加入1mL酶液,继续保温,在不同时间分别测定反应混合液流出粘度计小球的时间。对照实验采用经热处理已失活的酶液。
4.1.3 计 算
粘度下降百分数可用下式表示:
粘度下降(%)=100(To-T)/(To-Tα)(2)
式中:T、To和Tα分别为反应混合液、对照混合液和缓冲液的流出时间(s)。
酶溶液要预先稀释,使粘度降低范围在20%~80%。在此范围内,酶浓度对数与粘度降低率成正比。以酶作用时间为横坐标、粘度下降百分数为纵坐标做标准曲线,在图中查出粘度下降50%时对应酶的作用时间(T1/2)。在上述条件下,引起粘度下降50%的酶量为10个果胶酶活力单位,即酶活单位=10/(T1/2/3600)。
4.2 滴定法
4.2.1 原 理
果胶酶彻底水解果胶,生成半乳糖醛酸;半乳糖醛酸可与碘(过量)反应。反应后剩余的碘可用硫代硫酸钠溶液滴定,据此可得出酶解反应产生的半乳糖醛酸的量。以生成半乳糖醛酸的量衡量果胶酶的活力。
4.2.2 测定方法
取1%果胶溶液10mL,加入到5mL酶液和5mL水,调pH至3.5,在50℃水浴中保持2h,取出加热煮沸。冷却后,取5mL反应液移入碘量瓶中,加1M碳酸钠溶液1mL,0.1N碘液5mL,摇匀,加塞,于室温下放置20min,加2N硫酸2mL,用0.05N硫代硫酸钠滴定至淡黄色,加0.5%淀粉指示剂1mL,继续滴定至蓝色消失为止。记录所消耗的硫代硫酸钠毫升数A。空白试验用10mL果胶溶液、10mL水,不加酶液,不经保温,直接取此混合物5mL于100mL三角瓶中用于滴定,记录消耗的硫代硫酸钠毫升数B。
4.2.3 计 算
在上述条件下,1h酶促转化果胶、生成1mg当量游离半乳糖醛酸所需的酶量定为一个酶活单位。
每毫升酶液的活力单位=(B-A)N×0.51×20.(5×2×5)(3)
式中: N———硫代硫酸钠的当量浓度;
0.51———1mg当量硫代硫酸钠相当于0.51mg当量的半乳糖醛酸;
20———分解果胶反应液的总体积数;
5、2、5———分别表示反应中加入酶液的毫升数、反应时间、滴定时所取反应液的毫升数。
4.3 分光光度法
4.3.1 原 理
果胶酶分解果胶,产生带有还原性醛基的还原糖(以半乳糖醛酸计),一些显色剂可与其发生显色反应。根据颜色深浅的不同,可以通过分光光度计测定果胶酶酶活值的大小。本文以最常用的DNS比色法介绍此检测方法,其显色剂为3,5-二硝基水杨酸。
4.3.2 操作方法
取0.5%果胶溶液0.5mL加入到0.5mL酶液中,摇匀。在50℃水浴中准确反应0.5h,取出后,迅速在沸水浴中加热5min,冷却。取0.5mL反应液移入加有0.5mLDNS试剂的试管,加4mL蒸馏水,摇匀,在沸水浴中加热5min,迅速冷却。用分光光度计在540nm处测其吸光度值。参比液配制:加热灭活5min的0.5mL的稀释酶液与0.5mL0.5%果胶溶液充分混合。
4.3.3 计 算
采用标准曲线法,配制一系列已知浓度的标准葡萄糖溶液,在540nm处测定吸光度(A),以葡萄糖浓度(C)为横坐标、吸光度(A)为纵光标作A.C标准曲线(参见5.2节图2)。由标准曲线可得公式:
A=斜率×C(mg葡萄糖/mL)(4)
未知试液测定吸光度值A后,可通过上式求得C(mg葡萄糖/mL)。
在上述条件下,每小时内每毫升果胶酶酶促转化果胶生成1mg当量还原糖(以半乳糖醛酸计)所需的酶量定义为一个酶活单位。即:
果胶酶活(mg半乳糖醛酸/mL·h)=酶液稀释倍数×C(mg葡萄糖/mL)×2×194/180 (5)
式中: 194/180———葡萄糖换算成半乳糖醛酸的量;
2———测定中稀酶液被0.5%果胶溶液稀释的倍数。
4.4 3种方法的比较
将粘度降低法用来测定果胶酶的复合酶活力比较准确,但操作过程也相对复杂,且测定灵敏度不高。滴定法设备使用简单,测试重现行好,准确度高,但测定时间长,过程较繁琐,试剂用量较大。而分光光度法测定的灵敏度、准确度均高,重现性好,试剂用量少,尤其是操作省时、简便。对于上述3种测定方法,根据纺织行业的特点,笔者认为分光光度法更适于纺织工作者应用。下面重点探讨DNS比色法在实际应用中的一些具体问题。
5 应用DNS比色法测定果胶酶酶活
5.1 果胶溶液的配制以及酶液的稀释
果胶溶液的配制浓度以及酶液的稀释倍数是相互联系的两个数据,它们的确定对酶活测定结果的正确性起着关键作用。通过完成以下试验,可以确定有关参数条件。
5.1.1 材料与方法
5.1.1.1 仪器与试剂
UV—9200分光光度计;果胶(Sigma)、果胶酶制剂(NOVO)、3,5-二硝基水杨酸、巴比妥酸、巴比妥钠。
5.1.1.2 溶液配制
DNS试剂:将6.3g3,5-二硝基水杨酸、262mL2mol/LNaOH加到500mL含182g酒石酸钠的热水溶液中,再加5g苯酚及5g亚硫酸钠,待溶解、冷却后,加蒸馏水定容至1000mL,贮于棕色瓶中,一周后即可使用。
5.1.1.3 配制巴比妥缓冲液(pH=8.6)
称取1.84g巴比妥酸,置于56~60℃水中溶化,然后加入10.3g巴比妥钠,加蒸馏水定容至1000mL。
5.1.1.4 配制0.5%果胶溶液
准确称取0.5g果胶于烧杯中,用巴比妥缓冲液(pH=8.6)溶解、稀释定容至100mL。
5.1.2 制作果胶酶稀释倍数与吸光度关系曲线
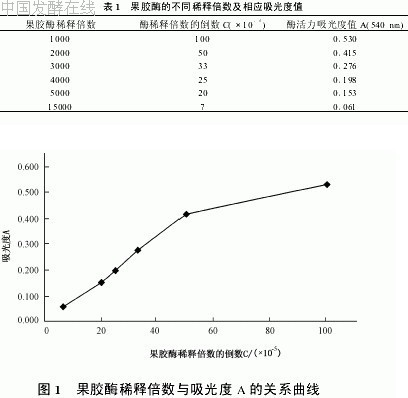
分别按表1的稀释倍数用蒸馏水稀释果胶酶,将稀释酶液按4.3.2测定吸光度值,以果胶酶稀释倍数的倒数为横坐标,吸光度(A)为纵坐标作关系曲线(见图1)。
5.1.3 结果与讨论
由公式(4)、(5)可得出,在酶活相同的情况下,吸光度与酶液稀释倍数的倒数应呈正比例关系。
图1为试验测得的果胶酶稀释倍数的倒数与其酶活力吸光度值关系曲线,从中可看出果胶酶的稀释倍数过低或过高都会偏离正比的线性关系,尤其在稀释倍数过低的情况下。原因可能有以下两点:①根据米氏学说,底物浓度应保持足够大到使酶饱和,达到最大反应速率,酶活值与酶浓度才能成正比。过高的酶液浓度可能使底物浓度相对不足,而不能满足这种正比关系。②根据朗伯-比耳定律,吸光度与浓度间只在一定范围内有较好的正比关系,酶促反应产生的高浓度产物与DNS的络合物颜色过深,会超过这一范围产生较大误差。稀释倍数过高时吸光度值也偏离朗伯-比耳定律,但仍满足底物使酶饱和的条件,因此产生的偏差相对小得多。果胶溶液的配制一定要有足够大的量,但过大的果胶浓度又会使溶液粘度加大,增加操作的误差。经过反复试验,在反应30min条件下确定0.5%的果胶浓度,效果最好。将表1的最高稀释倍数和最低稀释倍数的吸光度值删除,对其它数据进行回归分析,得到曲线的回归方程为:A=820.72C(R2=0.9943)。表明其线性相关度很好,说明当酶制剂稀释液的吸光度值在0.2~0.4范围内时,其酶活值有很高的准确度。用自产的粗酶液进行了同样的试验,也得到相同结果,因此,可以确定果胶溶液浓度为0.5%,控制酶液稀释倍数使吸光度值在0.2~0.4范围内。
5.2 葡萄糖标准曲线的绘制
绘制葡萄糖标准曲线的目的,也是找到葡萄糖溶液浓度与吸光度最佳线性关系的范围。绘制的参考数据及结果见表3、图2。由图2可见,在此范围内,曲线有较好的线性关系。
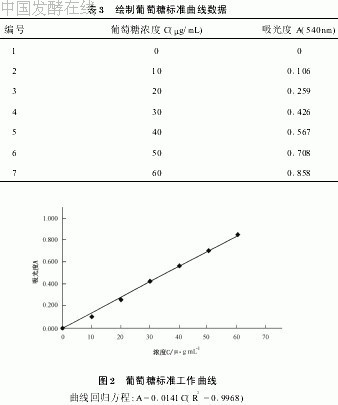
本测定方法采用葡萄糖绘制标准曲线,因为葡萄糖易得,且价钱便宜。用还原糖作为标准曲线,是为了标定果胶分解产生的还原性醛基的量。在公式(5)的求酶活公式中,有一项葡萄糖与半乳糖醛酸的转换系数,可换算为以半乳糖醛酸计。因此,无论用哪种还原糖作标准曲线,结果都是相同的。
5.3 试验温度和pH范围
酶促反应都有最佳反应温度和pH范围。在最佳酶反应范围内,酶作用的活力最高。最佳酶反应pH值和温度的范围是由酶的自身性质、特点所决定的,过多偏离此范围会使酶的活性降低甚至失去活性。因此在测定果胶酶活性时,作用温度和pH值要与其最佳反应条件范围相一致。最佳酶反应条件一般会由酶制剂厂家提供。在纺织领域应用的果胶酶,一般以碱性果胶酶为主。本试验应用的就是碱性果胶酶,其最佳反应条件是温度45~55℃,pH范围8~9。配制果胶酶溶液用巴比妥缓冲液(pH=8.6),在50℃水浴中进行酶促反应可获得最佳试验结果。
5.4 减少试验误差的两个要素
5.4.1 将灭活的酶液与同样量的、0.5%的果胶溶液混合,作为参比液,可以消除酶液及果胶溶液中所含微量还原性物质对测定值的干扰。这些干扰因素常会使被测酶活偏高。
5.4.2 酶促反应时间、温度条件必须严格控制,否则会产生较大误差。为减小误差,应特别注意以下两步操作:①果胶溶液先在50℃恒温水浴中预热5min。酶液在50℃恒温水浴中2min后,加入预热过的果胶溶液,迅速混合、记时。这样可使反应一开始就在50℃条件下进行。②酶促反应结束时,应迅速加热反应液,以终止反应。加热结束后,应迅速用自来水流冷却降温。