百里酚分光光度法测定发酵液中L-精氨酸含量
2007-10-25 10:00:56 来源:本站原创 评论:0 点击:
对发酵液中L-精氨酸含量的定量检测是L-精氨酸产生菌选育及发酵条件优化的重要内容之一。自Sakaguchi研究用α-萘酚的次氯酸钠溶液作为显色剂测定L-精氨酸以来,坂口反应(Sak-aguchi reaction)成为测定L-精氨酸最基本的原理[1],但该方法的显色产物颜色不稳定且背景颜色干扰较大,因此难以定量分析。许多文献报道了用其它显色剂作为改进的方法,但这些方法的精确度和准确度仍不理想[2~4]。本文采用百里酚的次溴酸钠溶液作显色剂,不仅能够克服用坂口试剂(Sakaguchi reagent)测定精氨酸时显色产物不稳定和背景颜色干扰大的缺点,而且操作简便、快速、灵敏度高、重现性好。
1材料与方法
1.1试剂
L-精氨酸:Sigma公司。百里酚、氢氧化钠、溴水、尿素等均为国产分析纯。
1.2仪器
UV-1700紫外分光光度计,日本岛津。其它均为实验室常用仪器。
1.3实验方法
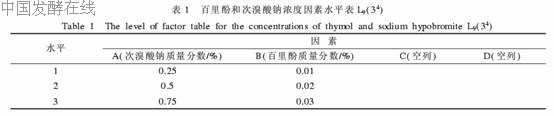
1.3.1显色液的配制百里酚溶液:分别称取0.10、0.20和0.30 g百里酚,溶于质量分数4%的NaOH溶液中,分别配成质量分数0.01%、0.02%、0.03%的百里酚溶液。次溴酸钠溶液:准确称取2.00 g纯溴水,溶于100 mL 5%NaOH溶液中,配制成2%的次溴酸钠溶液,用棕色试剂瓶冷暗处保存,用时以5%NaOH溶液稀释至质量分数分别为0.25%、0.5%和0.75%的次溴酸钠溶液。
1.3.2精氨酸标准溶液的配制精氨酸标准贮备液:准确称取50 mg L-精氨酸,加入蒸馏水配制成500μg/mL精氨酸贮备液。精氨酸标准溶液:准确吸取精氨酸标准贮备液,加入蒸馏水分别配制成5、10、15、20和25μg/mL精氨酸标准溶液。
1.3.3标准曲线的绘制准确吸取精氨酸标准溶
液和对照(蒸馏水)各5.0 mL,分别置于已编号的试管中,加入2.0 mL百里酚溶液,摇匀,置于冰水浴中,20 min后加入1.0 mL冷次溴酸钠溶液,迅速摇匀,溶液呈黄色,30 s内加入质量分数40%的尿素1.0 mL,摇匀,置于冰水浴中反应2 min,然后用分光光度计进行比色测定。根据精氨酸标准溶液的浓度和OD值绘出标准曲线,并列出标准曲线的回归方程。
2结果
2.1测定波长的选择
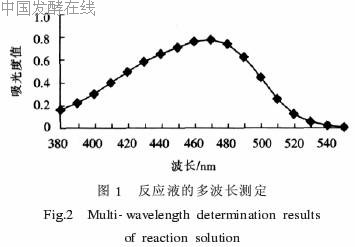
根据1.3.3节,用UV-1700型分光光度计对精氨酸与显色液的黄色反应液进行多波长测定。如图1所示,在470 nm处吸光值最大,因此,以470 nm作为反应液的测定波长。
2.2百里酚浓度和次溴酸钠浓度对标准曲线的影响
标准曲线的测定是根据精氨酸δ-胍基与坂口试剂反应后产生黄色物质的特殊性质,用分光光度计检测不同浓度精氨酸标准溶液与百里酚的次溴酸钠溶液的反应物的OD值,绘制精氨酸浓度与OD值关系的函数曲线。如标准曲线回归方程的相关系数足够高,可认为此标准曲线过原点。由此可知,标准溶液的OD值与标准曲线回归方程的斜率具有相关性,即标准溶液的OD值越大,标准曲线的斜率就越大。为了便于分析,以标准曲线回归方程斜率的变化表示标准曲线OD值的变化。
显色产物的OD值受百里酚和次溴酸钠浓度的影响。依据OD值较大且显色产物较稳定的原则来确定最佳的百里酚浓度和次溴酸钠浓度。在预实验的基础上,对不同浓度的百里酚和次溴酸钠溶液做全因素正交试验,因素水平见表1。
不同浓度的次溴酸钠和百里酚溶液与精氨酸标准溶液反应,标准曲线回归方程的相关系数均在0.9997以上,因此可以用标准曲线回归方程的斜率表示标准曲线的OD值。正交试验结果见表2。由表2可知,次溴酸钠浓度对标准曲线回归方程斜率影响大,百里酚浓度对标准曲线的斜率影响小,即影响标准曲线OD值的主要因素为次溴酸钠浓度,其次为百里酚浓度。对正交试验结果进行方差分析,结果见表3。由正交试验结果的方差分析可知,对标准曲线斜率的影响因素中,次溴酸钠浓度为极显著因素,百里酚浓度为不显著因素,且次溴酸钠浓度和百里酚浓度对标准曲线斜率的影响有交互作用,从而进一步说明了标准曲线的OD值主要由次溴酸钠浓度决定。次溴酸钠浓度和百里酚浓度的最佳值分别为A3(0.75%)与B3(0.03%),但是,百里酚质量分数从0.01%增至0.02%时,T1平均数和T2平均数的变化为0.0105,而其质量分数从0.02%变化至0.03%时,T2平均数和T3平均数的变化为0.00093,即后者对OD值的影响仅为前者的9%。也就是说,继续增加百里酚浓度对OD值的影响极小。另外,试验中发现,次溴酸钠质量分数为0.75%时,比色皿壁上有气泡,气泡过多会导致OD值读数不稳定,因此,次溴酸钠的质量分数不宜超过0.75%。为确定最佳百里酚和次溴酸钠浓度,分别对百里酚浓度和次溴酸钠浓度做单因素试验。
2.2.1次溴酸钠浓度对标准曲线影响的单因素试
验百里酚质量分数为0.03%、次溴酸钠质量分数分别为0.5%、0.6%和0.7%时,对次溴酸钠浓度
作单因素方差分析,如表4所示。
由表4可知,次溴酸钠质量分数分别为
0.5%、0.6%和0.7%时,标准曲线的斜率呈极显著性差异,并且当次溴酸钠质量分数从0.6%变化至0.7%时,标准曲线斜率的平均数变化较大,说明增加次溴酸钠浓度,吸光度值增加。0.7%次溴酸钠为其最佳质量分数。
2.2.2百里酚浓度对标准曲线影响的单因素试验
次溴酸钠质量分数为0.7%、百里酚质量分数为0.03%和0.04%时,对百里酚浓度作单因素方差分析,如表5所示。
由表5可知,当次溴酸钠质量分数为0.7%,百里酚质量分数从0.03%增至0.04%时,标准曲线回归方程的斜率变化不显著,即继续增加百里酚的浓度,吸光度值增加不显著,因此,根据正交试验方差分析结果,百里酚的最佳质量分数为0.03%。
2.3温度对标准曲线的影响
显色反应受温度的影响,不同温度下,显色产物的OD值不同[5~7]。当次溴酸钠质量分数为0.7%、百里酚质量分数为0.03%时,研究室温和冰水浴对标准曲线斜率的影响(见表6)。
试验结果表明,反应温度越高,标准曲线的斜率越小,即反应液的OD值越小。室温和冰水浴条件下,标准曲线的斜率呈显著性差异。因此,采用百里酚分光光度法测定L-精氨酸含量时,最好保持在冰水浴环境中。
百里酚分光光度法测定精氨酸含量的最佳条件为:次溴酸钠0.7%,百里酚0.03%,且反应液保持在冰水浴环境中。此条件下的标准曲线回归方程为:
y=0.03928x+0.00004(R2=0.9999)(1)
2.4发酵液中L-精氨酸含量的测定
将L-精氨酸产生菌的摇瓶发酵培养液稀释至5~20μg/mL。准确吸取稀释的发酵液各5.0 mL于试管中,加入2.0 mL 0.03%百里酚溶液,对照管中加入2.0 mL 4%NaOH溶液,摇匀,置于冰水浴中20 min,然后加入1.0 mL 0.7%冷次溴酸钠溶液,迅速摇匀,溶液呈黄色,测定方法同1.3.3节。根据标准曲线的回归方程和稀释倍数,计算发酵液中L-精氨酸浓度。
X=A×n1000×a(2)
式中:X———发酵液中L-精氨酸的质量浓度
(mg/mL);A———吸光度(OD470值);n———稀释倍
数;a———标准曲线回归方程斜率;1 000———由μg转化为mg的系数。
2.5精密度试验
测量方法的重现性对于准确测定发酵液中L-精氨酸是十分重要的。根据已确立的测定条件,连续5 d作平行测定,计算标准偏差和相对标准偏差,结果见表7。
3个发酵液样品的标准偏差分别为0.019、0.026和0.016,相对标准偏差分别为0.58%、0.59%和0.23%,说明该方法的精密度较高。
2.6回收率试验
为了考察本方法的准确度,对3批次的发酵液进行加标回收率试验,结果见表8。
因此应用分光光度法测定发酵液中L-精氨酸含量的准确度较高。
3讨论
(1)以百里酚的次溴酸钠溶液作为显色剂测定发酵液中L-精氨酸含量的最佳条件为:将发酵液质量浓度稀释至5~20μg/mL,取待测物稀释液5.0 mL,加入2.0 mL 0.03%百里酚溶液,然后加入1.0 mL 0.7%冷次溴酸钠溶液,迅速混合均匀,30 s内加入40%尿素1.0 mL,反应2 min,在波长470nm处比色测定。该反应在冰水浴条件下进行。根据式(1)和式(2)即可得出L-精氨酸浓度。
(2)次溴酸钠质量分数不能高于0.75%。随着次溴酸钠浓度的增加,标准曲线的斜率亦增加。当次溴酸钠质量分数为0.75%时,无论百里酚浓度的高低,比色皿壁上都出现气泡,此气泡可能是过量的次溴酸钠和尿素反应生成氮气所致。气泡过多使OD值不稳定,从而影响L-精氨酸测定的准确度和精确度,因此,次溴酸钠质量分数应低于0.75%。
(3)测定时,加入试剂的次序是:向待测物中
先加入百里酚溶液,使溶液混合均匀,然后加入次溴酸钠溶液,最后加入尿素溶液。试剂加入的顺序不能颠倒,否则不能形成稳定的黄色显色化合物。
(4)已加入百里酚溶液的待测物在冰水浴中添加次溴酸钠溶液后,剧烈震荡,混合均匀,使之显色;30 s内加入1.0 mL尿素,以中和过量的次溴酸钠,使显色稳定。在冰水浴条件下,如果不加入尿素,也有明显的腿色现象,导致OD值读数不稳定。
(5)测定标准曲线的OD值时,标准L-精氨酸的质量浓度不能超过25μg/mL,否则,不符合朗姆-比尔定律,不能准确测定发酵液中L-精氨酸的含量。发酵稀释液质量浓度在0~25μg/mL范围,该方法的检出限为2μg/mL,摩尔吸光系数ε
为6.8×103 L/(mol·cm)。
相关热词搜索:精氨酸
上一篇:“工程生物”生产抗菌肽的研究
下一篇:固态发酵产游离氨基酸的条件优化研究
评论排行
- ·中国发酵企业数据库(4)
- ·(4)
- ·CoQ10高产菌株选育的研究进展(2)
- ·抗生素发酵工艺所用冷却塔的性能分析及处理(1)
- ·微生物菌种选育技术.rar(1)
- ·发酵生产染菌及其防治(1)
- ·赤藓糖醇发酵工艺研究(1)
- ·重组AiiA 蛋白可溶性表达及发酵条件优化(1)
- ·生物反应器设计软件_发酵罐绿色版(1)
- ·酵母粉、酵母浸粉的区别(1)
- ·雷帕霉素研究进展(1)
- ·透明质酸用途和行业概况(1)
- ·黄酒制作工艺(1)
- ·水解(酸化)工艺与厌氧发酵的区别(1)
- ·糖蜜酒精废液处理过程中产生的微生物蛋...(1)
- ·紫杉醇高产菌发酵产物的分离、纯化和鉴定(1)